0%
昱展新藥(上櫃:6785)為台灣新藥研發公司,以 505 (b)(2) 為產品開發主軸,主要研發中樞神經系統疾病之新藥。公司於 2023 年創下台灣生技史上最大的授權案,從合作夥伴 Indivior 取得的研發和銷售里程金達新台幣 276 億元,看完這篇報告,你將了解以下 3 件事:
- 公司經營層及股權架構
- 505(b)(2) 競爭優勢分析
- 主要產品研發進程及未來潛力
註:505(b)(2) 是美國 FDA 申請新藥藥證的途徑之一,是將已經過 FDA 核准的藥品用新複方、新適應症、新使用途徑、新劑型和新劑量等方式重新上市
一、公司經營層及股權架構
董事長林東和及總經理文永順在生醫產業具豐富的經營經驗
董事長林東和及總經理文永順原先皆於美時(市:1795)任職(可參考:【關鍵報告】美時血癌藥 Lena 拓及全球,一文解析台灣營收最大的學名藥廠:美時),2016 年林東和跟文永順一同離開美時,創辦昱展新藥。
董事長林東和為台灣大學藥學系學士,具有超過 40 年生技製藥產業經驗,於 1966 年創立美時製藥,擔任美時董事長期間,成功讓美時上櫃,並轉型為國際學名藥廠。而總經理文永順為台灣大學化學所博士,具有超過 20 年生技製藥產業經驗,曾任美時製藥製劑開發處長。
製藥產業的豐富經驗,使昱展的經營團隊具備挑選藥品及合作夥伴的眼光,舉例而言,昱展選擇進入戒毒癮藥市場,便是因美時過去戒毒癮藥 Buprenorphine/Naloxone 銷售狀況極佳,看到此市場的潛力。此外,在挑選合作夥伴時,一開始的目標便是具有藥品製造及銷售能力的國際型垂直整合藥廠 Indivior ,加上 Indivior 為戒毒藥的原廠,故與其合作可以降低後續被提告的風險。
董事長林東和及總經理文永順兩人合計持股達 29.69%,由於兩人有豐富的醫藥產業經驗,富果判斷集中持股對公司未來發展有正面影響。
事長及總經理合計持股達 29.69%
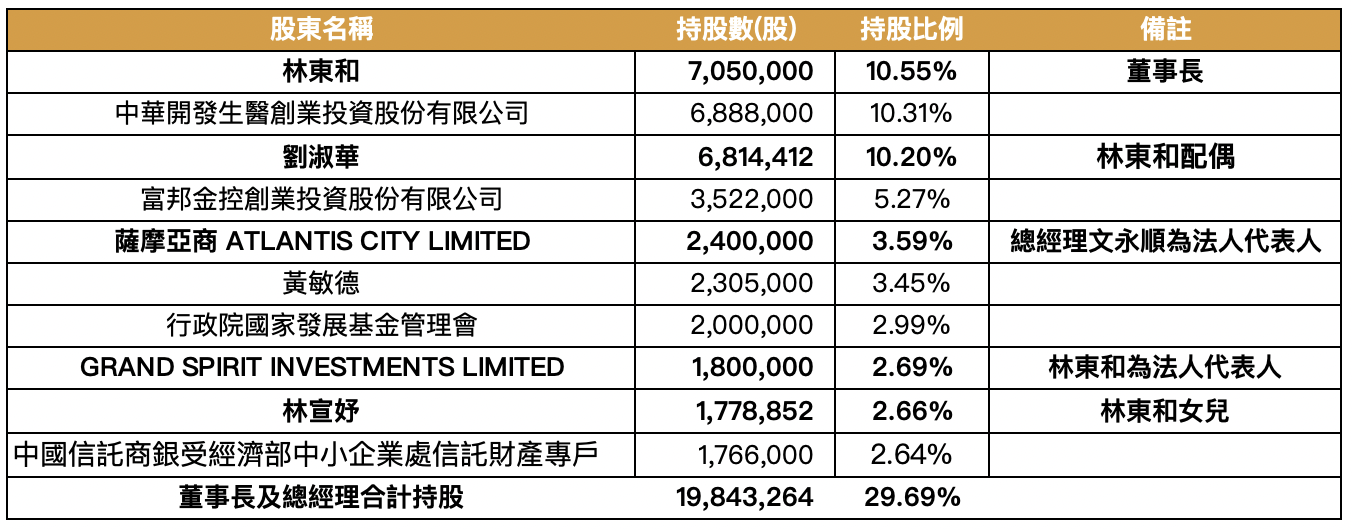 Source:昱展年報、富果研究部
Source:昱展年報、富果研究部
二、505(b)(2) 競爭優勢分析
鎖定 505(b)(2),並致力研發長效皮下注射劑
昱展鎖定 505(b)(2) 新劑型新藥進行研發,原因是此類型的藥物,相比
立即註冊會員閱讀全文10 秒註冊解鎖完整報告
10 秒註冊解鎖完整報告
每週更新,精準掌握投資決策
成為會員繼續閱讀全文,再享每週更新獨家研究報告與多項富果投資研究工具!
- 精選研究報告完整時事短評、法說會備忘錄
- 技術圖表多種投資分析工具與指標
- 筆記功能速記投資心得與重要筆記
- 自訂版面客製喜歡的看盤版面


